Ми з тобою однієї крові: Як людям пересаджують органи тварин
Американець Девід Беннетт страждав від невиліковного кардіологічного захворювання. Ситуація була настільки критична, що чоловік не міг претендувати на трансплантацію людського органу чи встановлення штучного серця. Тож Управління з санітарного нагляду за якістю харчових продуктів та медикаментів (FDA) видало дозвіл на «співчутливе використання» свинячого серця напередодні нового, 2022 року. Це формулювання застосовують тоді, коли експериментальне лікування — єдиний доступний варіант для пацієнта, який зіткнувся з небезпечною для життя недугою. На початку січня хірурги Медичної школи Мерілендського університету успішно провели операцію.
Історія вселяє надію, що одного разу органи тварин можна буде регулярно використовувати для пересадки людині. Це скоротить черги, в яких щороку помирають тисячі важкохворих пацієнтів, адже людських донорських органів просто не вистачає всім, хто потребує трансплантації.
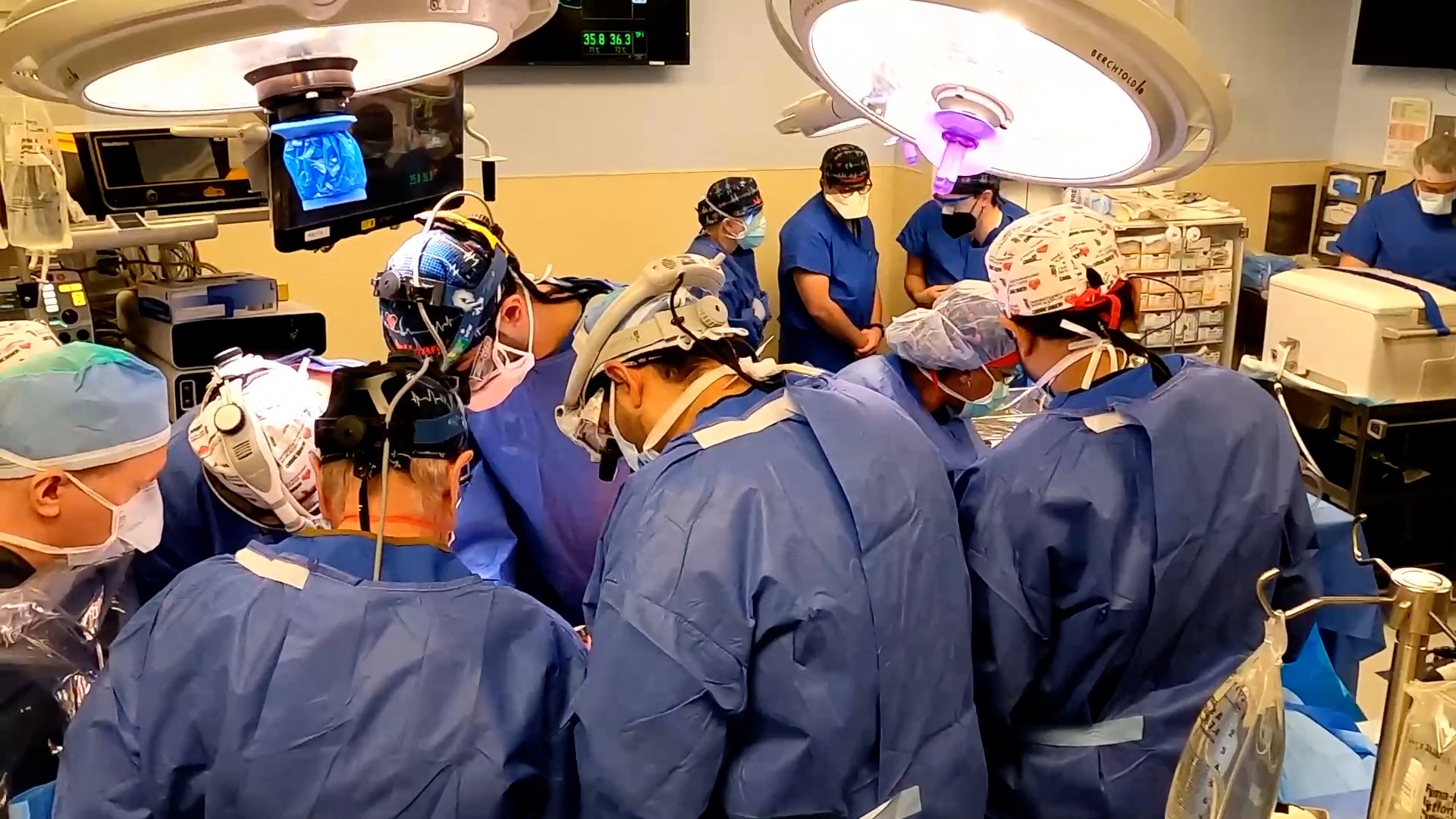
Та сама операція з пересадки серця 10 січня 2022 року. Фото: EyePress News / EyePress via AFP)
«Споріднені» донори
Пересадження людям органів, клітин і тканин тварин називається ксенотрансплантацією. Ще на початку ХХ століття кілька європейських лікарів пересаджували нирки кіз, овець, свиней та мавп людям. Усі ці спроби були неуспішними: пацієнти помирали невдовзі після операції.
Тоді медики ще не знали, що наша імунна система атакує чужорідні органи — навіть людські. Тому перед трансплантацією лікарі обов’язково оцінюють сумісність донора і реципієнта. На органи тварин імунна система реагує ще агресивніше, ніж на непідходящі людські. Це призводить до гострого відторгнення трансплантата.
Коли у другій половині ХХ століття з’явилися перші імунодепресанти — препарати для запобігання відторгненню, вчені знову зацікавилися ксенотрансплантацією. У 1960-х американський хірург Кіт Реемтсма пересадив нирки шимпанзе 13 людям. Більшість загинули за кілька тижнів після операції через реакцію відторгнення або інфекції. Але одна пацієнтка, 24-річна вчителька, прожила дев’ять місяців — певний час вона почувалася добре і навіть повернулася до роботи.
У 1960-х американський хірург пересадив нирки шимпанзе 13 людям. Більшість загинули за кілька тижнів.
У 1984 році хірург Леонард Лі Бейлі з Університету Лома Лінда в Каліфорнії пересадив серце бабуїна дитині, яка народилася зі смертельною вадою серця. Дівчинка, яка була відома як Бебі Фей, прожила 21 день. Ця операція викликала неоднозначну реакцію суспільства: багато хто звинувачував хірурга в неетичності. Але вона привернула увагу до проблеми нестачі донорських органів для дітей. Через рік Бейлі провів першу трансплантацію вже людського серця дитині.
Учені обрали приматів як потенційне джерело органів для ксенотрансплантації, оскільки вони — наші найближчі родичі. Найкращим варіантом вважали шимпанзе через оптимальний розмір органів та хорошу сумісність груп крові з людьми. Однак ці тварини незабаром були занесені до списку видів, що зникають.
До того ж при використанні приматів є підвищений ризик передачі захворювань. Адже ми, як споріднений вид, вразливі перед їхніми інфекціями — варто лише згадати про ВІЛ, який передався людям від мавп. Не можна забувати і про етичний бік питання. Чи правильно вбивати приматів заради людини?
Не лише м’ясо
Свиней як потенційне джерело органів почали вивчати у 1990-х роках. Цей вид і зараз вважається найбільш вдалим кандидатом для ксенотрансплантації. Переваги свиней — великий приплід, короткий період дозрівання, низький ризик зараження людини своїми інфекційними захворюваннями, а також наша фізіологічна схожість. Крім того, у свиней менше «етичний багаж», оскільки багато людей регулярно вживають у їжу свинину.
У свиней менше «етичний багаж», оскільки багато людей регулярно вживають у їжу свинину.
Перші експерименти розчаровували. Органи свині, пересаджені бабуїнам, відмовляли протягом кількох тижнів, незважаючи на імунодепресанти. У 1993 році хірург Девід Купер з Університету Піттсбурга в Пенсильванії виявив, що надгостра імунна реакція приматів, включаючи людину, спрямована на один антиген свині — молекулу вуглеводу, яка називається галактоза-альфа-1,3-галактоза, або скорочено альфа-гал.
Перша генетично модифікована свиня без альфа-гал була виведена 2003-го вченими з Revivicor. (Саме ця компанія згодом і надала серце свині для пересадки Девід Беннетту.) Нещодавно стали відомі ще дві вуглеводні молекули, що викликають гостру імунну реакцію, але Revivicor також вивела лінію свиней, у яких всі три небезпечні для ксенотрансплантації гени вимкнені.
До людини свинячі органи пересаджували і бабуїнам, проте найбільша тривалість життя тварини після трансплантації склала близько шести місяців. Команда вчених із Нью-Йоркського університету під керівництвом хірурга Роберта Монтгомері запропонувала інший підхід для досліджень. Так, наприкінці 2021 року медики провели дві операції з пересадки свинячої нирки пацієнтам, у яких було зафіксовано смерть мозку. Хірурги приєднали свинячу нирку до кровоносних судин стегна. Серцебиття, кровообіг та дихальну діяльність підтримували за допомогою штучної вентиляції легень. Протягом 54 годин, доки тривало спостереження, нирка працювала нормально. Лікарі не виявили жодних ознак відторгнення.
Віруси у ДНК
Свині мають один недолік, який значно підкосив дослідження ксенотрансплантації у 2000-х роках. Тоді стало відомо, що ендогенні ретровіруси свиней (PERV) можуть заражати клітини людини під час лабораторних експериментів. Ендогенні ретровіруси — це віруси, вбудовані у ДНК тварини. Вони безпечні для свого виду-господаря, але здатні активізуватися та викликати захворювання в іншого виду.
Більшість свинячих вірусів, бактерій і грибків усувають шляхом відбору неінфікованих тварин-донорів, розведення поросят у стерильних та ізольованих умовах. Але PERV входять до складу ДНК, і просто так їх не позбутися. Це стало можливим із появою нового методу редагування геному CRISPR-Cas9.
Перша свиня без ретровірусів народилася 2017-го. Дослідники компанії eGenesis назвали порося Лайкою на честь собаки-космонавта, яка вийшла на орбіту Землі у 1957 році. Учені вирізали за допомогою CRISPR-Cas9 усі 25 копій генів PERV. При цьому інші гени не були зачеплені.
Перша свиня без ретровірусів народилася 2017-го. Порося назвали Лайкою на честь собаки-космонавта, яка вийшла на орбіту Землі у 1957 році.
Існують розбіжності щодо того, чи повинні органи свині бути вільними від PERV для успішної трансплантації людям. Можливо, така модифікація не потрібна. На практиці у приматів, яким пересаджували органи свиней, жодного разу не зафіксували інфікування PERV.
Постачальник сердець
Компанія Revivicor, яка надала серце генетично модифікованої свині Девіду Беннетту, у 2003 році відокремилася від PPL Therapeutics, британської фірми, що свого часу прославилася
перший ссавець, клонований із клітини іншої тварини

Клонована вівця Доллі. Фото: Wikimedia Commons
У грудні Revivicor отримала схвалення Управління з санітарного нагляду за якістю харчових продуктів та медикаментів на використання свиней лінії GalSafe (тобто вони генетично модифіковані таким чином, щоб не виробляти альфа-гал). Але Revivicor також вирощує невелике стадо свиней із більш ретельною генною інженерією. У цих тварин уже цілих 10 генетичних змін — усе заради того, щоб їхні органи найкраще підходили для пересадки у тіло людини. Так, дослідники компанії виключили три гени, відповідальні за швидке відторгнення органів свині людським організмом. Крім того, вчені прибрали ще один свинячий ген, щоб запобігти росту тканини серця, і додали у ДНК тварини 6 людських генів для покращення сумісності донора й реципієнта.
У тварин уже цілих 10 генетичних змін — усе заради того, щоб їхні органи найкраще підходили для пересадки у тіло людини.
Саме свиня з цього особливого стада стала донором серця для Девіда Беннетта. За кілька годин до операції хірурги забрали серце тварини та помістили його у перфузійний бокс — інноваційний пристрій, який омиває орган спеціальним розчином. Бокс, розроблений шведською компанією XVIVO, дозволяє довше зберегти донорське серце і запобігти його пошкодженню. Також медики використали експериментальний імунодепресант від фармацевтичної компанії Kiniksa Pharmaceuticals.
Пересадка свинячого серця Девіду Беннетту, безумовно, знакова мить в історії ксенотрансплантації. Проте щоб пересадка органів тварин увійшла у звичайну медичну практику, можуть знадобитися роки. Лікарям необхідно зібрати ще багато інформації, щоб бути впевненими у безпеці та ефективності цього виду трансплантації.